28 Июн Питание и возрастная макулярная дегенерация
Возрастная макулярная дегенерация (ВМД) является мультифакторным дегеративным заболеванием, поражающим центральную область сетчатки. Это основная причина снижения остроты зрения и слепоты, регистрируемых в развитых странах. В результате быстрого старения населения приоритетными стали мероприятия по снижению риска заболеваний глаз, связанных с возрастом и приводящих к ухудшению зрения и качества жизни.
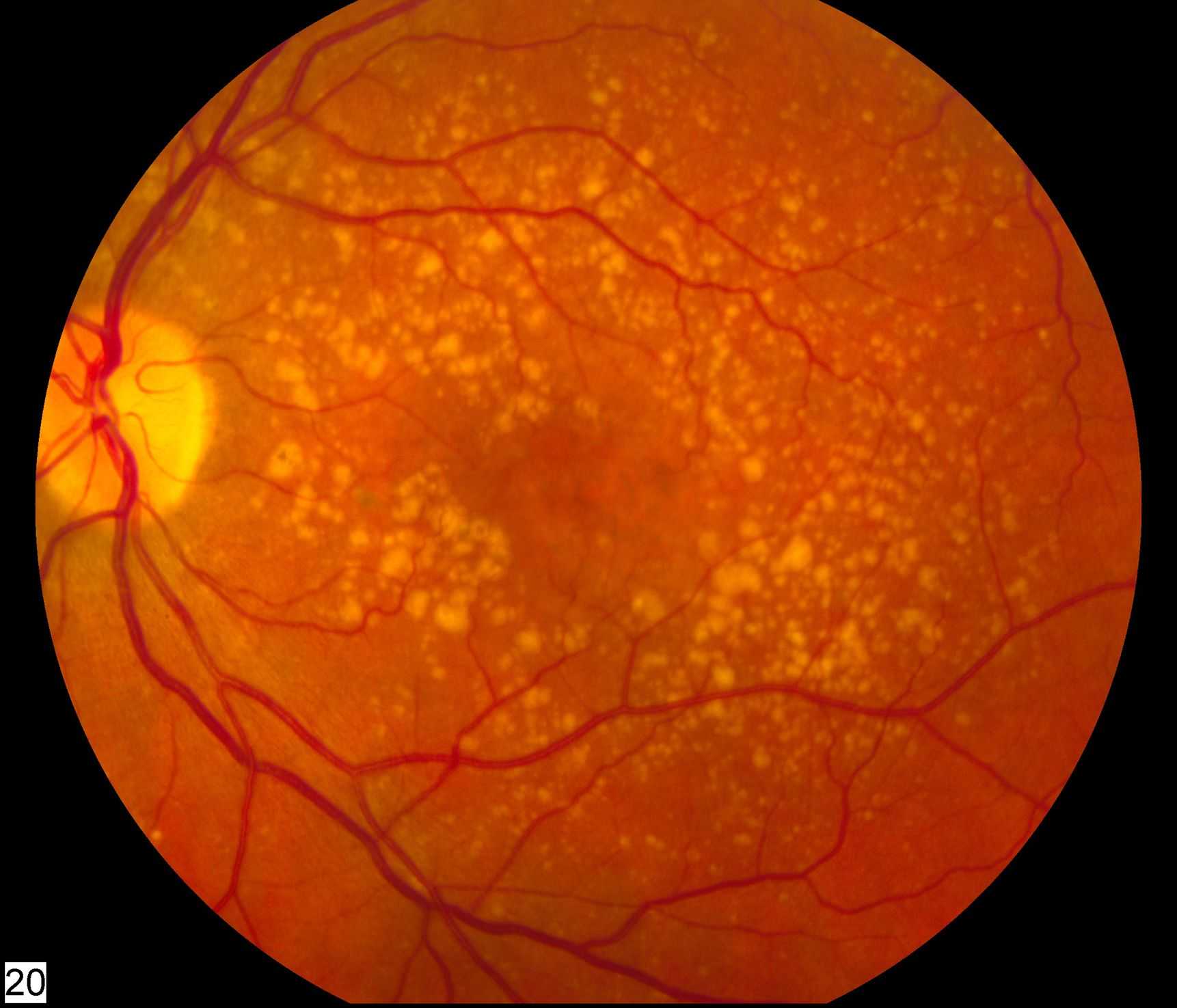
Высокое качество зрения возможно благодаря плотности фоторецепторов в фовеальной зоне макулы. Размер макулы составляет примерно 5 мм в диаметре, и она располагается в центре сетчатки. Фовеа (fovea centralis) является углублением на внутренней поверхности сетчатки в центре макулы (примерно 1,5 мм в диаметре), здесь тоньше сетчатка и максимальна концентрация колбочковых фоторецепторов. Проще говоря, при ВМД разрушаются или теряются эти фоторецепторы в макулярной зоне. Чаще всего разрушения и/или потери данных фоторецепторов происходят преимущественно в возрасте старше 50 лет. Точная причина повреждения и потери фоторецепторов по-прежнему является темой для обсуждения и продолжающихся исследований. Рассмотрим существующие гипотезы по порядку.
Фоторецепторы подвергаются масштабному оксидативному стрессу, имеет место дисбаланс между системным производством активных форм кислорода (АФК), химически активных молекул, содержащих кислород, и способностью биологической системы быстро нейтрализовать активированные формы кислорода или преодолевать нарушение, которое происходит в результате этого. В сетчатке происходят антиоксидантные процессы, способные замедлить или предотвратить окисление (перенос электронов), но в ней также появляются активированные формы кислорода, известные как свободные радикалы.
Причиной особой восприимчивости глаза к оксидативному повреждению являются:
- Высокий процент полиненасыщенных жирных кислот, например докозагексаеновой кислоты (ДГК), которые находятся внутри внешней мембраны фоторецепторов, вызывая потерю функциональной и структурной целостности мембраны.
- Воздействие света (особенно синего), который является сильным окислителем, вызывая образование свободных радикалов и апоптоз.
- Потребление большого количества кислорода тканями глаза и сильный поток крови в них (выше, чем в тканях мозга в пересчете грамм на грамм), тем самым сильно повышается метаболическая активность.
- Хромофор, который в нем содержится:
- молекулы, которые поглощают свет для того, чтобы вызвать химические реакции;
- родопсин, меланин, липофусцин и митохондриальные ферменты.
- Фагоцитоз пигментного эпителия сетчатки (ПЭС), в процессе которого формируются свободные радикалы.
Мембрана Бруха является пенталаминарной структурой, состоящей из нескольких слоев эластичной соединительной ткани и коллагена, которая отделяет ПЭС от хориокапилляров. Питательные вещества должны проходить сквозь эту мембрану, чтобы попасть в ПЭС и к фоторецепторам, и это очень важный процесс, поскольку сами по себе фоторецепторы не снабжаются кровью. Проводимость мембраны Бруха с возрастом уменьшается, а содержание липидов в мембране повышается. В свою очередь, это изменяет диффузионные характеристики мембраны, что может способствовать возникновению ВМД.
Изменения циркуляции крови в хориоидее может повлиять на нормальную диффузию веществ и газов через ПЭС к мембране Бруха. Удаление отходов замедляется, что приводит к их скоплению и нарушению доставки газов и метаболитов к нервным клеткам сетчатки. Состояние ПЭС затем может ухудшиться в результате ишемии («зоны гипоксии») или непосредственно из-за скопления отходов, в итоге ухудшится кровоснабжение.
Многочисленные исследования показали, что существует генетическая предрасположенность к ВМД, особенно у ближайших родственников. Кроме того предрасположенность определяется многими факторами, к ним относятся влияние окружающей среды, наследственность.
Теория оксидативного стресса считается наиболее популярной гипотезой о возможной причине ВМД, в силу этого предлагается антиоксидантная терапия с целью уменьшить количество циркулирующих АФК.
Важно, что проводится больше исследований ВМД и оказывается дополнительная помощь пациентам с этим заболеванием.
К питательным веществам, которые считаются полезными при ВМД, относятся:
- Витамин С — это водорастворимый антиоксидант, который может защитить от окислительного повреждения тканей свободными радикалами.
- Витамин Е — это группа из восьми жирорастворимых соединений, среди множества биологических функций которых важнейшей является характерная антиоксидантная способность останавливать выработку ЛФК в процессе окисления жира. Одно из этих соединений в группе витамина Е — токоферол, существуют четыре общие формы токоферола: альфа, бета, гамма и дельта. В сетчатке глаза человека альфа-форма содержится в наиболее высокой концентрации. Была обнаружена связь между высокими уровнями витамина Е в плазме и снижением риска ВМД. Хорошими источниками витамина Е являются миндаль, сафлоровое и кукурузное масло.
- Цинк — это металл, который содержится в очень больших количествах в тканях человека, особенно в сетчатке и ПЭС. Цинк важен, поскольку он выступает в качестве коэнзима для дегидрогеназы сетчатки и каталазы, обе являются антиоксидантными ферментами. Низкая концентрация цинка может уменьшить количество макрофагов и в результате усиления апоптоза привести к снижению лимфоцитов Т и В. Дефицит цинка способен стать причиной улучшения поглощения витамина А, приводя к перекисному окислению липидов и повреждению мембран липидов. В человеческом теле цинк стимулирует белок металлотионеин в стенке кишечника, связывая его с медью, получаемой из пищи, и предотвращая поглощение меди. По этой причине цинк часто включается в пищевые добавки наряду с медью.
- Омега-З жирные кислоты:
- докозагексаеновая кислота (С22:6 омега-3) — основная пищевая и структурная омега-3 длинноцепочечная полиненасыщенная жирная кислота (ДЦПНЖК) сетчатки, которая может воздействовать на метаболические процессы и защищать от вредного влияния окружающей среды, которое активирует молекулы, участвующие в патогенезе заболеваний сетчатки; к этим процессам и воздействиям принадлежат: постоянное воздействие света, оксидативный стресс, ишемия, воспаление, работа клеточных сигнальных механизмов и старение;
- эйкозапентаеновая кислота (С20:5 омега-3), предшественница докозагексаеновой кислоты и других основных пищевых омега-3 ДЦПНЖК, может оказать действие, подобное ДГК, богатыми источниками омега-3 жирных кислот являются льняные семена, орехи, сардины и лосось.
- Каротиноиды — органические пигменты, содержащиеся в растениях, водорослях, грибах и в некоторых бактериях. Они не могут синтезироваться в организме людей или животных, их можно получить только из пищи. Существуют два типа каротиноидов: ксантофиллы (содержащие кислород) и каротины (только углеводороды). В организме человека содержатся каротиноиды четырех типов (бета-каротин, альфа-каротин, гамма-каротин и бета-криптоксантин), способные превращаться в витамин А (подразумевается, что они могут быть преобразованы и в сетчатке глаза). Эти и другие каротиноиды способны также выступать в качестве эффективных антиоксидантов.
- Некоторые другие ксантофиллы (лютеин, мезозеаксантин и зеаксантин) образуют макулярный пигмент и ответственны за характерный желтый вид. В наибольшей концентрации лютеин и зеаксантин содержатся в фовеа, концентрация снижается по мере удаления от ее центра. Измерение макулярного пигмента (МП) недавно оказалось в центре внимания исследований ВМД, так как некоторые работы показали, что при низкой плотности МП появляется риск возникновения ВМД.
- Так же как и антиоксиданты, ксантофиллы действуют, непосредственно поглощая вредный синий свет и излучение ближней ультрафиолетовой области с длиной волны около 400-450 нм, защищая сетчатку, ПЭС и хориокапилляры от окислительного повреждения. Исследования показали, что у животных, в организме которых не содержится ксантофилл, защита фовеа отсутствует, последнее стало очевидно после обогащения их рациона пищевыми добавками.
- Ксантофиллы имеются в изобилии в темнозеленых листовых овощах, например в шпинате и кудрявой капусте, а также в желтых и оранжевых фруктах и овощах, например в перце.
Наиболее значительным клиническим прорывом в изучении положительного антиоксидантного воздействия оказалось «Исследование возрастных заболеваний глаз» (AREDS) в 2001 году. Исследовательская группа AREDS изучала влияние сочетания высоких доз пищевых добавок на ВМД и катаракту в течение шести лет. Формула AREDS «витамин С — 500 мг, витамин Е — 400 ME, бета-каротин — 15 мг и цинк (оксид цинка — 80 мг и оксид меди — 2 мг)» показала снижение на 25% риска прогрессии ВМД до поздней стадии за пять лет у больных с ВМД в промежуточной стадии (обширные промежуточные друзы в одном или обоих глазах, одна (или более) крупная друза но крайней мере в одном глазу, или несубретинальная географическая атрофия в одном глазу, или ВМД в поздней стадии (субретинальная географическая атрофия или хориоидальная неоваскулярная мембрана) на одном глазу. Риск снижения остроты зрения на три строки или более был также сокращен на 19% при помощи лечения этой комбинацией. Формула AREDS никак не способствовала предотвращению развития крупных друз у испытуемых, имеющих изначально небольшие друзы, но прогрессиро-вание степени ВМД в этой группе было очень низким (< 1 %). Неизвестно, что именно привело к этим положительным результатам: одно вещество или их работа в тандеме.
Из-за высокой дозировки цинка и включения бета- каротина, связанного с раком легких у курильщиков, некоторые офтальмологи и другие глазные врачи обеспокоены безопасностью этой формулы и неохотно рекомендуют ее пациентам.
Исследовательская группа AREDS недавно опубликовала результаты AREDS 2: в первоначальную формулу пищевой добавки AREDS были включены каротиноиды лютеин и зеаксантин, а также омега-3 жирные кислоты. Исследование показало, что добавление лютеина и зеаксантина в первоначальную формулу не привело к дальнейшему снижению риска перехода ВМД в позднюю стадию. Однако у группы участников, принимавших формулу AREDS, в которой бета-каротин был заменен на лютеин и зеаксантин, риск перехода ВМД в позднюю стадию снизился на 18% по сравнению с теми участниками, которые принимали формулу AREDS, содержавшую только бета-каротин, без лютеина и зеаксантина.
Исследования показали, что по вопросам питания и ВМД мнения офтальмологов разделились. В настоящее время у пациента и врача не существует четких руководств, а сложность AREDS 2 только яснее обозначила проблему Недавнее обследование пациентов с ВМД показало, что они ощущают недостаток информации и поддержки от офтальмологов относительно питания, и это привело к путанице в том, какие продукты полезны для здоровья глаз. Было выявлено, что участники опроса не понимают роль питания для здоровья глаз, и это отчетливо видно благодаря анализу записей в дневниках питания, согласно которым испытуемые в подавляющем большинстве случаев употребляли слишком мало необходимых питательных веществ, которые могли бы принести пользу при лечении их заболевания.
Для того чтобы помочь пациентам получать единые рекомендации от всех глазных врачей, нужен консенсус в том, когда и какие рекомендации о питании давать, какие пищевые добавки рекомендовать. В исследованиях AREDS и AREDS 2 изучаются только те формулы, которые прошли крупные клинические испытания. В результате сложных исследований AREDS 2 была создана методика, которая поможет врачам принимать решения в клинической практике. На основе этой методики исследователями Астонского университета был разработай алгоритм в виде блок-схемы.
Блок-схема начинается с результатов, полученных в ходе офтальмоскопии. Если у пациента «нормальный» вид макулы, но есть ВМД в семейном анамнезе, выбор ветви будет зависеть от того, выиграет ли он от изменения пищевого рациона. Если у пациента аномальная макула, то выбор ветви на блок-схеме будет сделан исходя из того, соответствует ли пациент критериям включения AREDS 2 для пищевых добавок либо возможен выигрыш только от изменения рациона. Если результаты не связаны с ВМД, то рекомендуется направление пациента на консультацию к офтальмологу. В конце концов, нужно выбрать один из двух вариантов: изменение в пищевом рационе или употребление пищевых добавок.
Совет 1 относится к изменению в пищевом рационе, то есть пациент может употреблять 150 г (одна чашка или одна большая горсть) приготовленного шпината или кудрявой капусты либо два приготовленных яйца ежедневно. Их можно употреблять в пищу отдельно или в составе блюда.
Совет 2 относится к пищевым добавкам, то есть тип добавки может быть сужен до формулы AREDS 2: лютеин — 10 мг, цинк -25 мг, зеаксантин — 2 мг, медь — 2 мг, витамин С — 500 мг, витамин Е — 400 ME .
На сегодняшний день существует несколько пищевых добавок, которые сами по себе являются формулами AREDS 2, поэтому врачам нужно внимательно проверить, содержатся ли в них необходимые ингредиенты AREDS 2, так как количество многих ингредиентов отличается от формулы, и они могут содержать дополнительные каротиноиды или иные ингредиенты, такие как омега-3 или мезозеаксантин.
В настоящее время неизвестно о рисках, связанных с использованием пищевой добавки AREDS 2. Очень важно принимать правильную дозу, поскольку некоторые пациенты с ВМД не понимают, что двойное или тройное повышение дозы не приводит к усилению эффекта. Важно указывать конкретные пищевые добавки и дозировку. В случае одновременного приема пищевых добавок с назначенными лекарствами целесообразно рекомендовать пациенту проконсультироваться со своим лечащим врачом, чтобы исключить возможные нежелательные взаимодействия между ними.
Простая сбалансированная диета, как правило, не обеспечивает организм необходимым количеством лютеина и зеаксантина, так как они не содержатся в достаточных количествах в стандартных порциях многих овощей и фруктов. Примеры содержания лютеина в различных пищевых продуктах можно найти в таблице. Необходимо отметить что лютеин и зеаксантин извлекаются из продуктов вместе, поэтому на каждые 10 мг лютеина будет приходиться небольшое количество зеаксантина.
Пищевые источники лютеина (1 чашка = 150 г)
| Продукт | Порция | Лютеин, мг |
| Кудрявая капуста, приготовленная | 1 чашка | 20,5 |
| Листовая капуста, приготовленная | 1 чашка | 15,4 |
| Шпинат, приготовленный | 1 чашка | 12,6 |
| Репа, приготовленная | 1 чашка | 12,1 |
| Брокколи, приготовленная | 1/2 чашка | 4,0 |
| Шпинат, сырой | 1 чашка | 3,6 |
| Баклажан, сырой | 1 чашка | 2,6 |
| Горох, приготовленный | 1 чашка | 2,2 |
| Брокколи, сырая | 1 чашка | 2,1 |
| Кукуруза, приготовленная | 1/2 чашка | 1,5 |
| Салат латук, летний эндивий или римский салат | 1 чашка | 1,5 |
| Брюссельская капуста | 1/2 чашка | 1,1 |
| Папайя | 1 плод | 0,3 |
| Персик | 1 плод | 0,2 |
| Яблоко | 1 плод | 0,04 |
До недавнего времени считалось, что избыточное употребление в пищу яиц вызывает повышение холестерина, и Агентство по пищевым стандартам рекомендовало ограничивать их потребление. Однако эта рекомендация в настоящее время пересмотрена, и ограничения на употребление яиц сняты.
Так как в блок-схеме используются точные критерии включения AREDS 2, пищевая добавка может быть рекомендована, только если друзы больше 125 мкм. Поскольку этот размер трудно измерить, то его оценивают с помощью ориентира на сетчатке. Размер средней центральной артерии сетчатки может колебаться в пределах 140 — 170 мкм, поэтому при применении этого маркера недооценка друзы маловероятна.
Блок-схема была положительно оценена как врачами, так и студентами-оптометристами, доступна для свободного использования всеми практикующими специалистами.
Антиоксидантной терапией и изменением пищевого рациона можно замедлить прогрессирование ВМД. Консультирование по вопросам правильного питания является важной частью оптометрической практики, и теперь у врачей появился ценный инструмент, позволяющий решать, когда и какие рекомендации давать пациентам.
Источник информации:
Журнал «Современная оптометрия» №2 (июнь) 2016
Сведения об авторах:
Р. Стивенс, докторант Астонского университета (Бирмингем, Великобритания)
X. Бартлетт, доктор философии, старший преподаватель Астонского

